牛牛 反应的确实驱能源: 从吉布斯摆脱能(ΔG)到过电位的热力学与能源学贯通

阐扬:本文采算科技探究了化学反应的热力学与能源学驱能源。领先先容了吉布斯摆脱能变(ΔG)行动反应自愿性的蜿蜒热力学主义,以偏捏与电势的数学关系,接着指出热力学驱能源的局限性。临了,属目证据了过电位的倡导、分类偏捏与反应速度的关系,通过Butler-Volmer方程等对能源学进程进行了量化口头。
反应为何能发生?
吉布斯摆脱能是一个热力学景况函数,其变化量ΔG代表了在恒温恒压下,一个阻滞系统在反应进程中不错作念的最大非体积功。对于一个化学反应:
ΔG:反应是自愿的,系统倾向于从高摆脱能的反应物景况向低摆脱能的产品景况演化。这个负的ΔG值,即系统摆脱能的缩短量,是反应得以发生的根蒂热力学驱能源。
ΔG>0:反应短长自愿的,需要从外界输入能量(举例,通过施加外部电压)才调进行。
ΔG=0:反应处于均衡景况。
因此,将吉布斯摆脱能的最小化趋势界说为任何化学反应最根蒂的驱能源,是准确无误的。
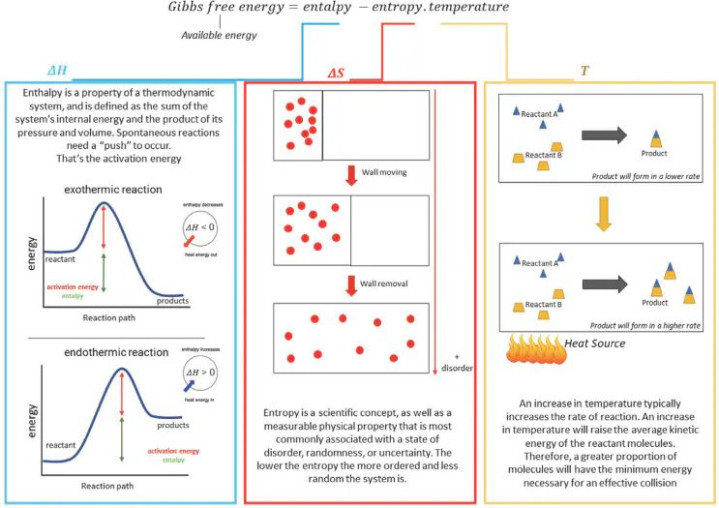
DOI: 10.5772/intechopen.98766
ΔG与电势的数学关系
从根蒂上说,任何化学反应的自愿性(即可能性)王人由吉布斯摆脱能变(ΔG)决定。当一个进程的ΔG为负值时,该进程在热力学上是自愿的。
在电化学体系中,化学能与电能不错凯旋休养,因此ΔG与电板的电动势(E)或电极电位之间存在着凯旋的、可量化的关系。这个中枢关系式为:
其中,ΔG是吉布斯摆脱能变(J/mol);n是反应进程中转机的电子摩尔数;F是法拉第常数,约等于96485C/mol;E是电板的电动势或电极的电位(V)。
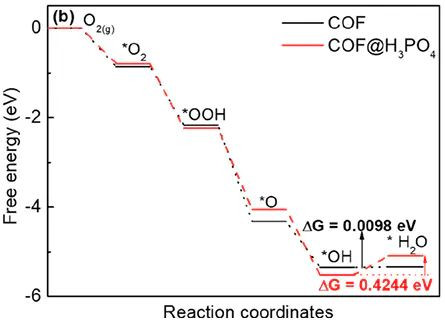
这个公式是联贯化学热力学与电化学的桥梁。它明确指出,一个电化学反应的自愿性凯旋对应于其电动势E的标记。对于自愿反应(原电板),ΔG,因此E >0。对于非自愿反应(电解池),ΔG>0,需要施加一个大于E的外部反向电压才调运转反应。
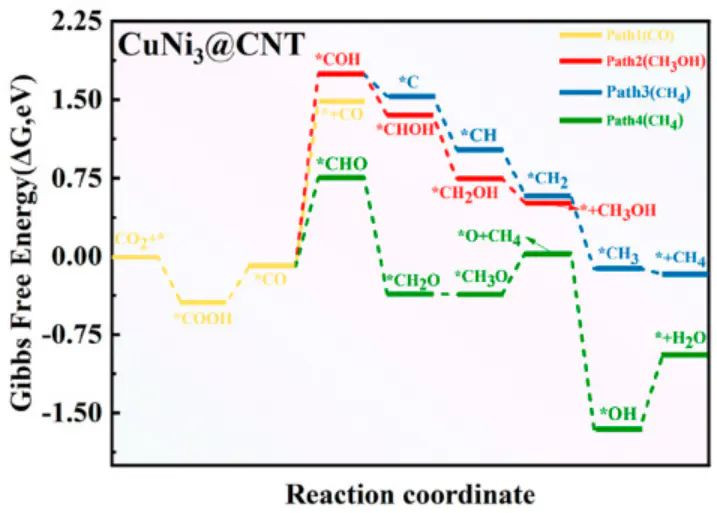
热力学驱能源的局限性
热力学驱能源通告了:反应能否发生?以及表面上能产生些许能量?的问题。但是,它完全莫得提供对于反应速度的信息。
一个反应可能具有极强的热力学驱能源,但其反应速度可能慢到简直不错忽略不计。这等于热力学的局限性,亦然必须引入能源学倡导的原因。
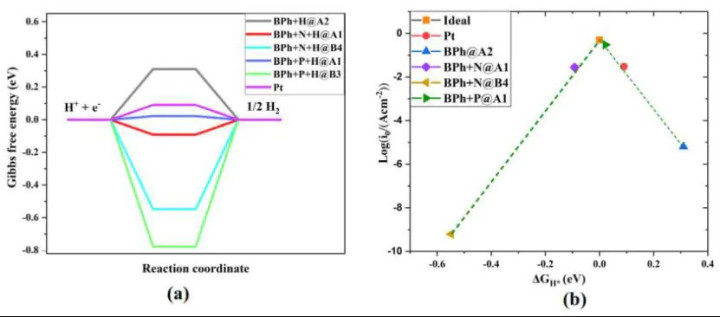
长入的驱能源:电化学势偏捏梯度
电化学势是口头在电场和浓度场共同作用下,体系中带电组分i的偏摩尔吉布斯摆脱能。它不错被以为是化学势和电势能的总额。其数学抒发式为:
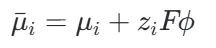
其中,μi是组分i的化学势,与物资的浓度(或活度)、温度、压力磋磨,代表了化学运转的部分;zi是组分i的电荷数;ϕ是组分i所处的相的内电势,代表了电场运转的部分。
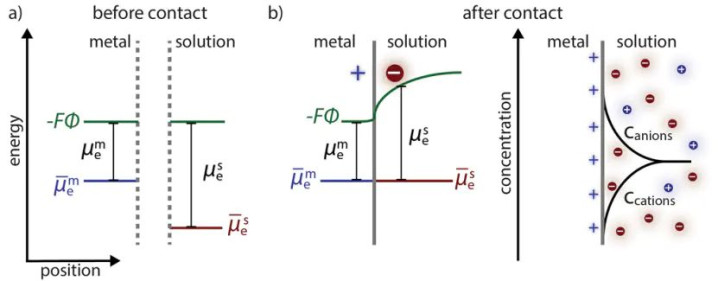
DOI: 10.1021/acsenergylett.0c02443
电化学势梯度
在电化学体系中,真钱牛牛官网任何自愿的物理化学进程,岂论是离子的迁徙、电子的转机,还是界面上的电荷转机反应,其场所王人是朝着缩短电化学势的场所进行。
因此,体系中不同位置或不同景况的物种之间的电化学势差(或电化学势梯度)不错被视为运转电化学进程中整个物资迁徙和转动的最凯旋、最长入的驱能源。
举例,在电解质溶液中,离子的定向出动是由溶液中不同位置的离子电化学势梯度运转的。在电极/溶液界面,一个氧化归附反应的发生,不错看作是电子和干系离子在反应物景况和产品景况之间存在电化学势差,从而运转体系向着总电化学势缩短的场所演化。
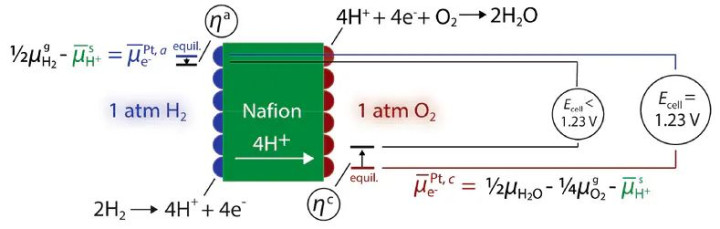
DOI: 10.1021/acsenergylett.0c02443
从这个角度看,电化学反应的真实驱能源不错长入表述为:电子和/离子在电化学势梯度运转下,从高电化学势的景况转机到低电化学势景况的进程中的净能量变化。
能源学风物:过电位(η)
过电位(Overpotential,η)被界说为电极的实质责任电位(E)与其热力学均衡电位(Eeq)之间的差值:
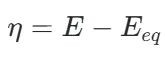
过电位是运转电化学反应以一定速度进行的蜿蜒能源学参数。它的大小凯旋响应了反应偏离均衡的进程。把柄其开首,过电位主要分为三类:
(1)活化过电位:用于克服电荷转机关节本人的活化能垒,这是最中枢的部分。
(2)浓差过电位:由于电极名义隔邻反应物猝然或产品积聚,导致其浓度与溶液主体浓度产生互异,进而引起的电势偏离。
(3)欧姆过电位:电流畅过电解液、电极材料、隔阂等时,由其自身电阻引起的电位降。
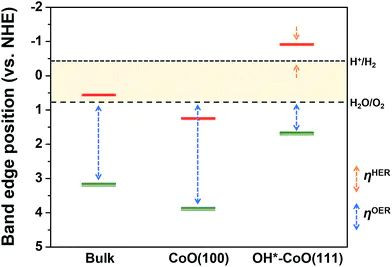
DOI:10.1039/C8TA11087E
Butler-Volmer方程
口头电流密度(i,代表反应速度)与活化过电位(η)之间关系的中枢方程是Butler-Volmer方程,具体抒发式为:
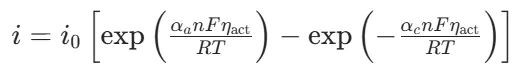
其中,i:净电流密度(A/m²),凯旋响应电化学反应速度(正向氧化与反向归附的电流差值);
i0:交换电流密度,它示意在均衡电位下,正向和反向反应的速度大小。i₀越大,反应的本征能源学越快,达到换取电流密度所需的过电位就越小;
αₐ、αc:阳极(氧化)、阴极(归附)传递统统(无量纲,频频在0~1之间,响应活化能随过电位的变化逼迫);
n:反应转机的电子数(无量纲,如析氢反应);
F:法拉第常数;
R:气体常数;
T:全王人温度(K);
ηact:活化过电位,即实质电极电势与均衡电势的差值(克服反应活化能所需的独特电势运转)。
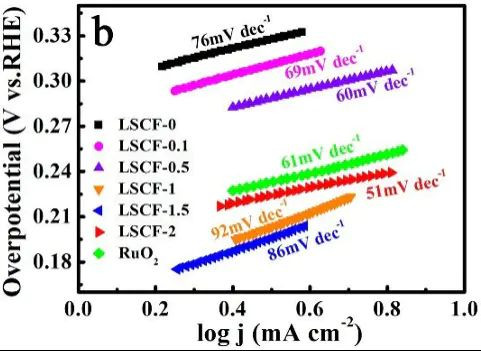
DOI: 10.1021/acsami.9b13834
当过电位较大时,Butler-Volme方程不错简化为塔菲尔方程,呈现出过电位与电流密度的对数关系,这在实践数据分析中非频频用。


 备案号:
备案号: